2018年5月北京北生研生物制品有限公司批簽發產品共3402860瓶,其中麻腮風聯合減毒活疫苗批簽發748190瓶,Sabin株脊髓灰質炎滅活疫苗(Vero細胞)批簽發1490580瓶,口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞)批簽發1164090瓶。
2018年5月北京北生研生物制品有限公司生物制品批簽發產品情況
生產企業 | 產品名稱 | 規格 | 批號 | 簽發量 | 簽發結論 |
北京北生研生物制品有限公司 | 麻腮風聯合減毒活疫苗 | 復溶后每瓶0.5ml。每一次人用劑量為0.5ml,含麻疹和風疹病毒均應不低于3.0LgCCID50,含腮腺炎活病毒應不低于3.7LgCCID50 | 201712067 | 124780瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 麻腮風聯合減毒活疫苗 | 復溶后每瓶0.5ml。每一次人用劑量為0.5ml,含麻疹和風疹病毒均應不低于3.0LgCCID50,含腮腺炎活病毒應不低于3.7LgCCID50 | 201712070 | 123990瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 麻腮風聯合減毒活疫苗 | 復溶后每瓶0.5ml。每一次人用劑量為0.5ml,含麻疹和風疹病毒均應不低于3.0LgCCID50,含腮腺炎活病毒應不低于3.7LgCCID50 | 201712068 | 125640瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 麻腮風聯合減毒活疫苗 | 復溶后每瓶0.5ml。每一次人用劑量為0.5ml,含麻疹和風疹病毒均應不低于3.0LgCCID50,含腮腺炎活病毒應不低于3.7LgCCID50 | 201712069 | 124200瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201802025 | 98604瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201802026 | 100254瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201803027 | 99024瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201803028 | 100104瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201803029 | 98724瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201803030 | 99714瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201803031 | 99924瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201803032 | 98124瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201803033 | 99804瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201803034 | 99594瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201803035 | 99834瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 麻腮風聯合減毒活疫苗 | 復溶后每瓶0.5ml。每一次人用劑量為0.5ml,含麻疹和風疹病毒均應不低于3.0LgCCID50,含腮腺炎活病毒應不低于3.7LgCCID50 | 201801001 | 124360瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 麻腮風聯合減毒活疫苗 | 復溶后每瓶0.5ml。每一次人用劑量為0.5ml,含麻疹和風疹病毒均應不低于3.0LgCCID50,含腮腺炎活病毒應不低于3.7LgCCID50 | 201801002 | 125220瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞) | 每瓶1.0ml(10人份)。每1次人用劑量為2滴(相當于0.1ml),含脊髓灰質炎活病毒總量應不低于6.12 lgCCID50,其中Ⅰ型應不低于6.0 lgCCID50,Ⅲ型應不低于5.5 lgCCID50。 | 201801014 | 83160瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞) | 每瓶1.0ml(10人份)。每1次人用劑量為2滴(相當于0.1ml),含脊髓灰質炎活病毒總量應不低于6.12 lgCCID50,其中Ⅰ型應不低于6.0 lgCCID50,Ⅲ型應不低于5.5 lgCCID50。 | 201801015 | 82950瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞) | 每瓶1.0ml(10人份)。每1次人用劑量為2滴(相當于0.1ml),含脊髓灰質炎活病毒總量應不低于6.12 lgCCID50,其中Ⅰ型應不低于6.0 lgCCID50,Ⅲ型應不低于5.5 lgCCID50。 | 201801016 | 82920瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞) | 每瓶1.0ml(10人份)。每1次人用劑量為2滴(相當于0.1ml),含脊髓灰質炎活病毒總量應不低于6.12 lgCCID50,其中Ⅰ型應不低于6.0 lgCCID50,Ⅲ型應不低于5.5 lgCCID50。 | 201801018 | 82470瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞) | 每瓶1.0ml(10人份)。每1次人用劑量為2滴(相當于0.1ml),含脊髓灰質炎活病毒總量應不低于6.12 lgCCID50,其中Ⅰ型應不低于6.0 lgCCID50,Ⅲ型應不低于5.5 lgCCID50。 | 201801019 | 82710瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞) | 每瓶1.0ml(10人份)。每1次人用劑量為2滴(相當于0.1ml),含脊髓灰質炎活病毒總量應不低于6.12 lgCCID50,其中Ⅰ型應不低于6.0 lgCCID50,Ⅲ型應不低于5.5 lgCCID50。 | 201801020 | 83130瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞) | 每瓶1.0ml(10人份)。每1次人用劑量為2滴(相當于0.1ml),含脊髓灰質炎活病毒總量應不低于6.12 lgCCID50,其中Ⅰ型應不低于6.0 lgCCID50,Ⅲ型應不低于5.5 lgCCID50。 | 201801021 | 83610瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞) | 每瓶1.0ml(10人份)。每1次人用劑量為2滴(相當于0.1ml),含脊髓灰質炎活病毒總量應不低于6.12 lgCCID50,其中Ⅰ型應不低于6.0 lgCCID50,Ⅲ型應不低于5.5 lgCCID50。 | 201801022 | 83460瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞) | 每瓶1.0ml(10人份)。每1次人用劑量為2滴(相當于0.1ml),含脊髓灰質炎活病毒總量應不低于6.12 lgCCID50,其中Ⅰ型應不低于6.0 lgCCID50,Ⅲ型應不低于5.5 lgCCID50。 | 201801023 | 83340瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞) | 每瓶1.0ml(10人份)。每1次人用劑量為2滴(相當于0.1ml),含脊髓灰質炎活病毒總量應不低于6.12 lgCCID50,其中Ⅰ型應不低于6.0 lgCCID50,Ⅲ型應不低于5.5 lgCCID50。 | 201801024 | 83280瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞) | 每瓶1.0ml(10人份)。每1次人用劑量為2滴(相當于0.1ml),含脊髓灰質炎活病毒總量應不低于6.12 lgCCID50,其中Ⅰ型應不低于6.0 lgCCID50,Ⅲ型應不低于5.5 lgCCID50。 | 201801025 | 82740瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞) | 每瓶1.0ml(10人份)。每1次人用劑量為2滴(相當于0.1ml),含脊髓灰質炎活病毒總量應不低于6.12 lgCCID50,其中Ⅰ型應不低于6.0 lgCCID50,Ⅲ型應不低于5.5 lgCCID50。 | 201802026 | 83490瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞) | 每瓶1.0ml(10人份)。每1次人用劑量為2滴(相當于0.1ml),含脊髓灰質炎活病毒總量應不低于6.12 lgCCID50,其中Ⅰ型應不低于6.0 lgCCID50,Ⅲ型應不低于5.5 lgCCID50。 | 201802027 | 83460瓶 | 予以簽發 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰質炎減毒活疫苗(人二倍體細胞) | 每瓶1.0ml(10人份)。每1次人用劑量為2滴(相當于0.1ml),含脊髓灰質炎活病毒總量應不低于6.12 lgCCID50,其中Ⅰ型應不低于6.0 lgCCID50,Ⅲ型應不低于5.5 lgCCID50。 | 201801017 | 83370瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201803037 | 101664瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201803036 | 99594瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201803038 | 97224瓶 | 予以簽發 |
北京北生研生物制品有限公司 | Sabin株脊髓灰質炎滅活疫苗(Vero細胞) | 每瓶0.5ml,每1次人用劑量為0.5ml。含脊髓灰質炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201803039 | 98394瓶 | 予以簽發 |
數據來源:中國食品藥品檢定研究院,智研咨詢整理
2018年5月北京北生研生物制品有限公司批簽發產品類型占比分布圖
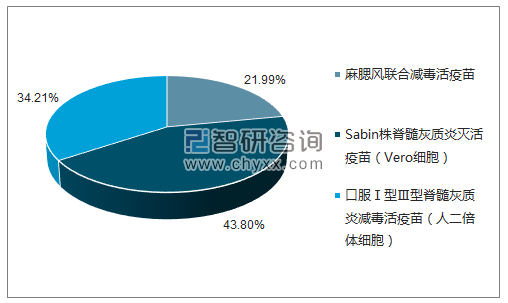
數據來源:中國食品藥品檢定研究院,智研咨詢整理

 公眾號
公眾號
 小程序
小程序
 微信咨詢
微信咨詢























